临床试验的质量事关药物研发能否获批,稽查是发现质量风险并进行控制的不可或缺的关键管理环节。监查、稽查、检查都是临床试验质量保证体系中紧密联系的质量管理行为,但高质量的稽查不是监查的集成或重复,也不应该是现场检查的预演,稽查是促进临床试验质量达到更高水平的重要途径。
随着国内临床试验质量管理理念的深化发展和质量监管要求的不断提高,稽查工作越来越被临床试验各方所重视,对于稽查工作的质量需求也越来越迫切,对稽查人才能力水平的要求也逐渐上升。高水平的稽查是基于一定的临床试验方案设计或解读能力,以及丰富的临床试验实践经验指导下的感性认知和理性实施。高水平的稽查人才能够对临床试验实施过程中可能出现的风险有良好的预判感知力,对隐藏在表象下深层次问题有敏锐的洞察力,并对发现的问题能够追根溯源,进而提出可行的解决方案。
然而如何才能成为一名优秀的临床试验稽查人才呢?
作为一名稽查或质量岗位的新人,您是否迫切希望获得高人指点迷津,打好基础快速入门?为此,我们精心准备了本次的初级课程,旨在帮助新人快速打好知识框架基础,建立质量体系观念实现快速入门。
作为有一定经验的稽查或质量经理,您是否迫切希望自己的稽查能力能更上一层楼,以突破久久不能攻克的职业瓶颈?为此,我们后续将推出稽查人才的中级课程,旨在帮助有一定经验积累的稽查从业人员梳理知识与能力框架,促进能力由量变向质变发展。
作为临床开发的管理干部,您是否为临床开发项目的质量担忧?又是否为如何基于科学性和临床运营的客观风险,做好研究质量管理的顶层设计而举棋不定?为此后续准备了稽查人才的高级课程,旨在帮助高级稽查或质量管理人员拓展视野,构建顶层设计能力,该班级拟采用最新创新案例教学闭门授课。
为促进稽查人才进阶和临床试验行业发展,中国药科大学将于7月底至8月初期间在南京举办“慧明临床试验稽查员培训班”,培训结束颁发中国药科大学结业证书,欢迎垂询。本课程是由众多专家老师,呕心沥血去芜存菁设计而成,含高级、中级、初级三套课程,追求理论结合最新实践。专家老师们为此付出了巨大努力,目标是赋能学员打造精品课程。该课程有以下两大特色:
特色一:课程摈弃从理论到理论浮光掠影的一般培训方式,授课老师专家均来自临床试验的一线,实战经验丰富,对临床试验的质量管理细节、案例能够信手拈来,坚持实用性、接地气的教学定位。
特色二:摒弃传统的稽查培训课程仅仅局限于稽查流程化工作等的局限性设计,而是将临床试验的质量管理看成一个系统性工作;从方案设计到执行,从科学性到规范性、真实性,从监管规则到逻辑分析等等进行的系统课程设计,确保学员能形成一个体系化的思维。
办班初心——帮助学员搭建系统化的知识体系,培训严谨的逻辑思考能力,了解熟悉临床试验设计、实践、管理的每一个环节。通过培训学习,让学员收获成长,最终助力中国新药创制。
二、组织机构
主办单位:中国药科大学继续教育学院
协办单位: 南京引光医药科技有限公司
三、时间地点
开班时间:因专家日程与原定开班时间冲突,更改为2023年7月29日-30日或2023年8月5日-6日(准确开班时间后续另行通知)
地点:中国药科大学(南京市鼓楼区童家巷24号)
四、培训对象
稽查员或业内拟学习临床试验质量管理的人员,本班次注重基础,重点针对入行2年以内人员或拟从事稽查工作的初学者。(有意向学习高级稽查员课程及精英稽查员课程的学员朋友,可关注后续通知)
五、名师风采
教学师资——有二十余年的临床试验设计、机构质量管理经验的业内著名学者,也有临床试验现场检查的资深检查专家,还有征战稽查现场多年的高级职业稽查实战高手等。名师领军,兼具理论高度与实战经验:

李正奇
博士、主任药师、教授
历任CFDA药品认证管理中心处长
CDE外聘专家
16年CFDA GCP/GLP现场检查组织管理工作经历
全程组织参与了“722”核查
组织参与了临床试验机构管理与现场检查等十余项法规的撰写工作
作为主编或执行主编出版了《药物临床试验机构管理指南》、《药物临床试验管理学》、《生物等效性试验实用指南》等著作。

蒋 萌
主任医师、教授、博士研究生导师
国家药监局审评中心审评专家
国家药监局审核查验中心检查员
主持Ⅰ~Ⅳ的药物临床试验项目方案设计和实施几十项
参加国家药监局审核查验中心数据现场核查项目几十项
历任江苏省中医院机构办公室主任兼临床药理科主任、科技处处长兼GCP中心主任
现任江苏省中医院GCP中心临床试验技术总监
现任中华中医药学会临床药理专委会副主任委员
现任南京药学会药物临床试验专业委员会主任委员
主编出版《药物临床试验机构管理实践(上下册)》、《I期药物临床试验质量管理实践》、《中医药临床研究实践》等著作。发表药物临床试验论文20余篇。

王慧萍
副主任医师
国家药监局/江苏省药监局药物临床试验项目核查专家
南京药学会临床试验专业委员会副主任委员
南京药学会理事会理事
江苏省药学会促进医药产业发展专业委员会名誉顾问
江苏省医学会医学伦理学分会委员会委员
出版专著:《药物临床试验机构管理实践》、《新版GCP法规和技术培训考核实用题典》等著作
承担科技部GCP平台建设课题1项,主持省级课题2项
六、培训事项
1.报名二维码:

3.汇款单位账号信息:
收款单位:中国药科大学
开户银行:南京工行湖南路支行
银行账号:4301011019001029831
转账备注:慧明临床试验稽查培训班
4.住宿事宜:交通费及住宿费自理。
5.中国药科大学继续教育学院联系人:
董雪松:13505180632;电子邮箱:1500965321@qq.com
且 奕:15005167979;电子邮箱:qy19941125@hotmail.com
中国药科大学继续教育学院
2023年06月12日
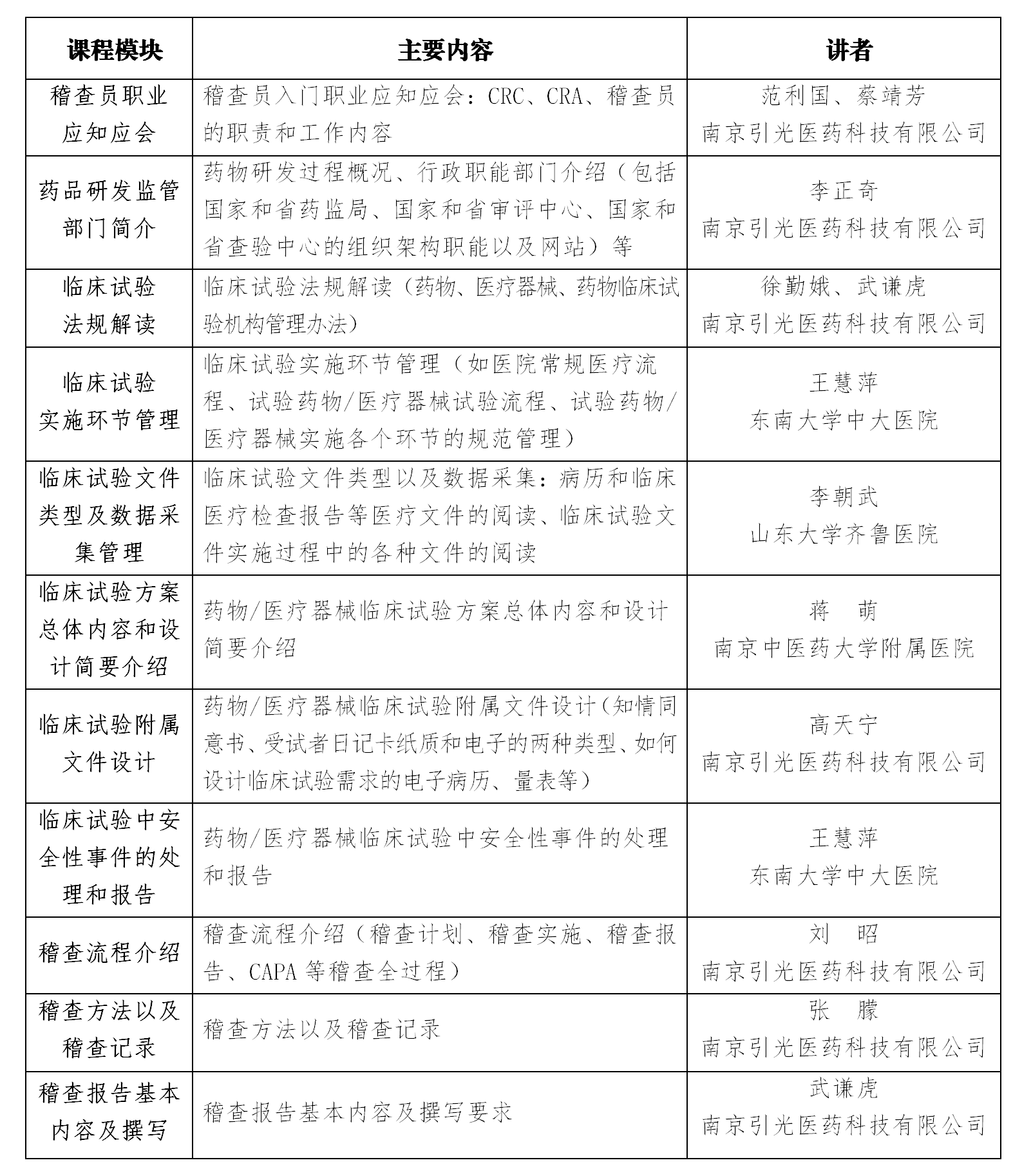
附件:《2023年第一期慧明临床试验稽查员培训班》课程安排表